6 Das vegetative Nervensystem VNS. und die Psyche
Emotionen und Stress können sich negativ auf Herz und Kreislauf auswirken und zu Krankheiten führen. Der Vagusnerv, ein Zweig des vegetativen Nervensystems (vgl. Abb. 4), kann einen psychogenen Herzstillstand auslösen. Der Vagusnerv ist verantwortlich für die Versorgung des inneren Verdauungstrakts, des Herzens und der Lunge und steuert alle anderen inneren Organe. Wie schon Rüegg beschreibt, besteht das VNS aus drei Teilen, dem Sympathikus, seinem Gegenspieler dem Parasympathikus (zu dem der Vagusnerv gehört) und dem Darm-Nervensystem. Letzteres besitzt über 100 Millionen Nervenzellen (Neuronen), viel mehr als sich im Rückenmark befinden. (Rüegg J C, 2003)
6.1 Der Vagusnerv
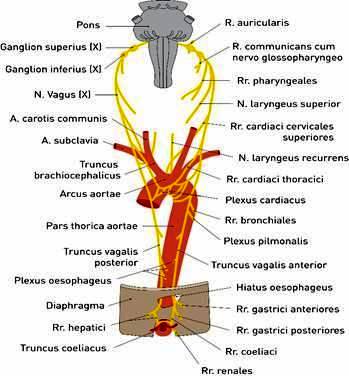
Abb. 4: Vagusnerv
Modifiziert übernommen aus Putz R, Pabst R (2000), S. 274
Der Vagusnerv ist der X. Hirnnerv und hat nicht nur eine vegetative Funktion, sondern ist auch an der motorischen Steuerung von verschiedenen Organen wie Kehlkopf, Rachen und obere Speiseröhre beteiligt. Er übermittelt Geschmacksempfindungen vom Zungengrund und Berührungsempfindungen aus dem Rachen, dem Kehlkopf und einem Teil des Gehörgangs.
6.2 Das vegetative Nervensystem und seine zwei untergeordneten Mechanismen
Dazu gehören Sympathikus, Parasympathikus und Vagusnerv
Kurze anatomische Beschreibung
Der Sympathikus entspringt dem Rückenmark im Brust- und Lendenbereich und verläuft weiter entlang der Wirbelsäule. Er aktiviert den Körper für Höchstleistungen. Wie schon Rüegg erklärt, steigt der Puls im Fall einer Erhöhung der Sympathikusaktivität bis auf das Fünffache und es kommt zu einer Erhöhung des Blutdrucks.
Im Gegensatz dazu kann der Parasympathikus, der Gegenspieler des Sympathikus, durch seine Funktion einen Herzstillstand verursachen. Nur durch Harmonisierung von Sympathikus und Parasympathikus entstehen regelmäßige Pulsrate und allgemein positive Organfunktionen. (Rüegg J C, 2003)
Das vegetative Nervensystem wird auch als autonomes System bezeichnet, da seine Steuerung unwillkürlich und unbewusst erfolgt. Ein typisches Beispiel ist mentaler Stress bei einer mündlichen Prüfung. Der Sympathikus wirkt ohne unseren Willen. Das Stresshormon wird erhöht und blockiert die Gedächtnisareale im Gehirn. Es kommt zu einem vorübergehenden Aussetzen des Gedächtnisses („Black-out“) und ebenso zu einer kurzfristigen Durchblutungsstörung des Herzmuskels (transiente Ischämien des Myokards). Dies ist z.B. der Fall bei einer arteriosklerotischen Verengung der Herzkranzgefäße, die eventuell zu einem Herzinfarkt führt.
Emotionen, wie Ärger, Freude, Furcht, Wut, etc, sind mit Gefühlsregungen verbunden und äußern sich in Gestik, Mimik, Körperhaltung und Stimme und werden auch durch das VNS gesteuert. Selbst die Hautdurchblutung wird emotional durch den Sympathikustonus reguliert, Blässe im Fall eines Schrecks oder Röte im Wutanfall veranschaulichen diesen Prozess.
Willkürliche oder unwillkürliche Bewegungen sowie Muskelanspannung oder -entspannung entstehen, wie schon Rüegg beschreibt, durch Aktivierung des Sympathikus bzw. Parasympathikus und lösen eine Frequenz elektrischer Impulse (Aktionspotenziale) aus. (Rüegg J C, 2003)
Diese werden in Salven von den Sympathikusnervenzellen entlang der sympathischen Nervenfasern zur glatten Muskulatur der Blutgefäße bzw. zum Herzen und zur Herzmuskulatur weitergeleitet. Auf diese Art wird durch die sympathischen Nervenfasern Noradrenalin freigesetzt. Die Frequenzrate liegt bei 2-8 Salven pro Sekunde. Die Überreaktionen des sympathischen Nervensystems werfen eine Art Spiegelbild auf die Muskeltätigkeit. Überdies werden alle Handbewegungen, selbst solche, die nur in Gedanken stattfinden, vom Sympathikus aktiviert. In einem Experiment (Vissing und Hjortso, 1996) wurde Nervengift in einen Unterarm injiziert um den Muskel zu lähmen. Dennoch fand bei der Muskelanspannung eine Aktivierung des Sympathikus statt. Somit wurde bewiesen, dass diese Aktivität durch das Gehirn und nicht durch die Muskelanspannung ausgelöst wurde. Für unsere Vorfahren war diese automatisierte Reaktion von Vorteil. Sie waren dadurch auf Kampf und Flucht gut vorbereitet. Vergleichsweise leben die Menschen heute mit viel weniger Kampf- und Fluchtsituationen. Unverarbeiteter Stress beeinflusst das Herz-Kreislauf-System negativ.
Der schweizer Nobelpreisträger Walter R. Hess prägte den Begriff „Abwehrreaktion“. Er bewies durch ein Tierexperiment – einer wachen Katze wurden schwache Stromstöße im Hypothalamus, im unteren Teil des Zwischenhirns, versetzt – dass die Katze Wut und Abwehrverhalten zeigte und es zu einem Anstieg ihres Blutdrucks kam.
Wie schon Rüegg erklärt, werden einige unwillkürliche und vegetative Körperfunktionen, wie etwa die Körpertemperatur, durch den Hypothalamus kontrolliert (vgl. Abb. 5). Der Mandelkernkomplex, die corpora amygdaloidea, die durch Nervenbahnen mit dem Frontalhirn verbunden ist, überwacht die Aufgaben des Hypothalamus. Er ist auch Teil des limbischen Systems und liegt über dem Zwischenhirn. (Rüegg J C, 2003)
Die corpora amygdaloidea ist der Ort an dem die Emotionen entspringen. Er bewertet und leitet Meldungen von den Sinnesorganen kommend, hinsichtlich ihres Charakters wie z.B. in Gefahrensituation, sehr schnell weiter, sogar noch vor dem Bewusstwerden der Gefahr. Psychosozialer Stress, der mit Emotionen wie Furcht, Ärger und Wut verbunden ist, aktiviert beim Menschen die Abwehrreaktion. Diese wird über Sympathikus und Hypothalamus eingeleitet.
6.2.1 Gliederung des Gehirns in seine Hauptabschnitte
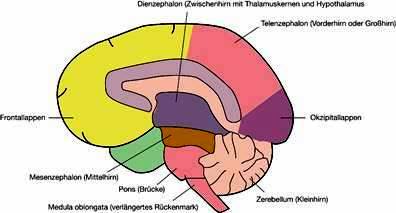
Abb. 5: Gliederung des Gehirns in seine Hauptabschnitte
Die linke und die rechte Hirnhemisphäre des Großhirns werden von den Hirnhäuten umhüllt, in ihrem Inneren enthalten sie die mit Liquor gefüllte rechte und linke Hirnkammer. Modifiziert übernommen aus: Rüegg J C, 2003, S. 3
6.2.2 Der Sympathikus und sein Gegenspieler der Parasympathikus
Der Sympathikus wird aktiviert durch unbewusst emotionale Reaktionen bei der Kampf- und Abwehrreaktion, bei körperlicher Belastung, Wut und Angst.
Beim Menschen bewirkt der Sympathikus eine Mobilisierung der Energiereserven, um eine außergewöhnliche Leistung zu ermöglichen. Somit wird auch das Herz-Kreislauf-System aktiviert. Alle Organe die unter dem Einfluss des Sympathikus stehen, tun dies auch gleichzeitig unter der Wirkung seines Gegenspielers, des Parasympathikus. Dieser entspringt im Kreuzmark, erreicht von dort aus die Beckenorgane und verläuft durch das Rückenmark bis zum Hirnstamm. Der wichtigste parasympathische Hirnnerv ist der Vagus, der “Umhergehende”, er kontrolliert nicht nur das Herz, sondern den gesamten Verdauungstrakt.
Wie schon die Bezeichnung “Gegenspieler” andeutet, führt der Parasympathikus, im Gegensatz zum Sympathikus, zu einer Erholungsphase im Organismus. Dadurch werden Herzfrequenz und Blutdruck gesenkt.
Bei Harmonie zwischen Sympathikus und Parasympathikus befindet sich das vegetative Nervensystem in einem ausgewogenen Zustand. Bei labilen Menschen, die an einer vegetativen Dystonie leiden, kommt es zu einem Überschuss an parasympathischen bzw. sympathischen Reaktionen. Im Falle eines ausgeprägten Sympathikotonus herrscht Nervosität. Im Gegensatz dazu wird, wie schon Rüegg erwähnt, bei einem Überschuss an parasympathischer Aktivität auf eine chronische Ermüdung (Chronic-Fatigue-Syndrom) geschlossen. Der Parasympathikus verstärkt die Darm-Tätigkeit, wenn sie durch den übergroßen Sympathikotonus gestört wird. Bei einer Unterdrückung von Ärger kann der Parasympathikus gehemmt werden. Dies kann zu einer Verstopfung führen.
(ebd.) .
Sympathikus
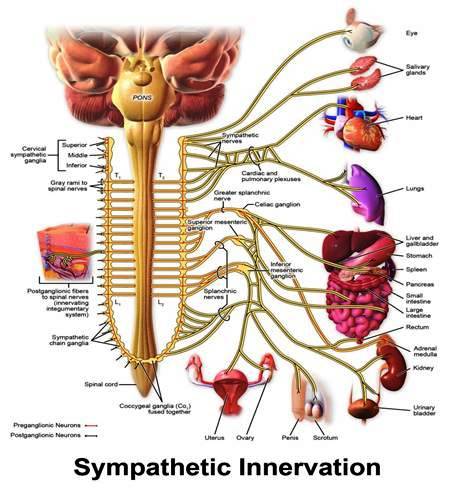
Der Sympathikus besteht aus 100 Millionen Neuronen (entscheidend mehr als im Rückenmark) und wird durch instinktive, emotionale Reaktionen aktiviert. (Rüegg 2003). Während der vegetativen Steuerung bei Emotionen wie z.B. bei Angst, Stress und Wut, puffert das Stresshormone mehr Konzentrat ins Blut, wodurch eine Übersäuerung entsteht, welches einen Einfluss auf die Dysfunktionalität der Neurotransmittersysteme hat. Somit kann dies ein Auslöser für psychische Erkrankungen sein. Der Sympathikus wirkt als Mobilisierung des Energiehaushaltes, um eine außergewöhnliche Leistung erbringen zu können, wie z.B. beim Sport oder auch bei Kampf- und Fluchtverhalten. Somit wird das Kreislaufsystem mit allen körperlichen Organen angeregt.
Sympathetic innervation
6.2.3 Pyramidenbahnsystem und Extrapyramidalbahnsystem als Teil des vegetativen Nervensystems (VNS)
Im Rückenmark verlaufen zwei Nervenstränge: Es sind dies die Pyramidenbahn (absteigende Bahn, vgl. Abb. 6) und die Extrapyramidalbahn (aufsteigende Bahn) des VNS.
Wie schon Rüegg erklärt, werden die Nervenzellen des sympathischen Astes, die im Rückenmark liegen, über die Pyramidenbahn von Neuronen in der Medulla oblongata (ein Teil des Hirnstamms) erregt. Letztere wiederum wird von hierarchisch übergeordneten Hirnzentren beeinflusst. Die Pyramidenbahn ist der Hauptteil des Pyramidalen Systems (PS). Auf der unteren Seite der Medulla oblongata verlaufen die Fasern beidseitig des Rückenmarks.
Zwischen Rückenmark und Nachhirn kreuzen 70-90% der Neuriten auf die jeweils andere Seite (Pyramidenkreuzung Decussatio pyramidum).
Im Vorderstrang des Rückenmarks laufen die restlichen Neuriten (Tractus corticospinalis anterior paramedian) und kreuzen in die kontralaterale Seite des Rückenmarks. Der Rest bleibt ungekreuzt und verläuft ipsilateral.
Die Interneuronen im Rückenmark werden vom PS gezogen und über die motorischen Vorderhornzellen gesteuert. Einige Fasern gehen direkte Verbindungen ein, die sogenannten monosynaptischen Verbindungen (ebd.).
Parasympathikus
Der Parasympathikus ist verantwortlich für seine parasympathische Neuronen und ihre prä- und postganglionäre Verschaltung. Die prä-und postganglionäre Verschaltung findet im parasympathischen Ganglion in kleiner Form statt. Dieser Prozess befindet sich in der Nähe der Organversorgung durch die vegetative Innervation. Die Signalvermittlung entsteht durch Acetylcholin. In Vergleich mit der Sympathikus-Innervation werden die Neurotransmitter von dem postganglionären Parasympathikus in den Organen freigesetzt.
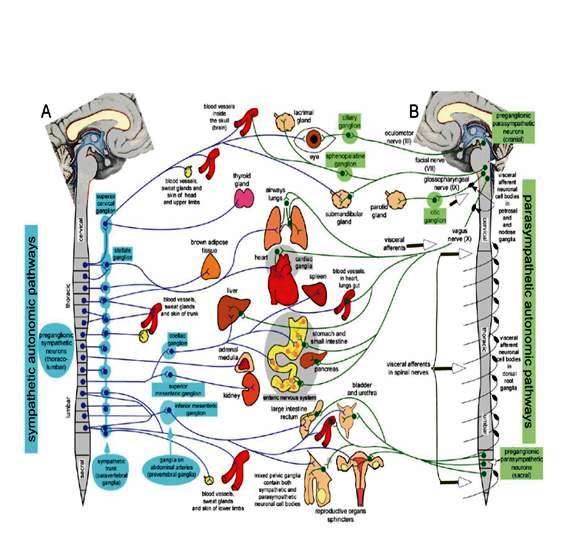
Schematischen Darstellung Parasympathikus
Abb. 13: Parasympathikus und Sympathikus in verschiedenen Organen
Quelle: https://bit.ly/2HxjHuvhttps://bit.ly/2HxjHuv
Die Korrelation zwischen Gehirn und Immunsystem beeinflussen die Immunzellen mit ihren Interleukinen über den afferenten Vagus. Dahingegen reagiert das Gehirn durch die Reize des Immunsystems mit einer Reaktion der Nebennierenrinden-Achse, dem Hypothalamus und den Hypophysen. Durch dieses Verfahren ergeben sich Feedback-Mechanismen von einer überschießenden Immunreaktion. Dadurch können Entzündungen geheilt oder gedämmt werden. Wenn das Kortisolkonzentrat PH-Wert niedrig in die Blutbahn gepufft wird, übersteigert sich die Immunreaktion, weshalb in Therapien bei Autoimmunerkrankungen mit Zusatz von Kortisolkonzentrat behandelt wird (Rüegg 2001).
Rückenmark mit Pyramidenbahnsystem und Extrapyramidalbahnsystem als Teil des vegetativen Nervensystems VNS
Abb 6: Pyramidenbahnsystem (absteigende Bahn) als Teil des vegetativen Nervensystems
Modifiziert übernommen aus Kahle W, Leonhardt H, Platzer W, (1979), S. 283
6.2.5 Das vegetative Nervensystem übermittelt Signale
Wie schon Rüegg beschreibt, geben die Rückenmarkneuronen über Axone (nervale Fortsätze) vom Gehirn empfangene Botschaften an die sogenannten sympathischen Ganglien weiter, die außerhalb des Rückenmarks liegen
(vgl. Abb. 7).
Der periphere Sympathikus, die gemeinsame Endstrecke vom Rückenmark zum Zielorgan, besteht aus Ketten von jeweils zwei Nervenzellen, den präganglionären und postganglionären Sympathikusneuronen. Diese sind durch Synapsen (neuronale Kontakte) miteinander verbunden, welche aus den zwei einander gegenüberliegenden Zellmembranen der sich berührenden Neuronen und auch dem submikroskopisch schmalen synaptischen Spalt bestehen.
Die Membran vor dem Spalt wird als präsynaptisch, die andere als postsynaptisch bezeichnet. In der Synapse kommt es zu einer synaptischen Übertragung von chemischen Substanzen von präganglionären auf postganglionäre Nervenzellen. Der chemische Stoff, der als Acetylcholin bezeichnet wird, wird bei Erregung über die Nervenendigungen der präganglionären Neuronen durch elektrische Impulse (Aktionspotenziale) übertragen und freigesetzt.
Nachdem Acetylcholinmoleküle die präsynaptische Zellmembran passiert haben, verbreiten sie sich auf die gegenüberliegende Seite des synaptischen Spalts und erreichen innerhalb einer tausendstel Sekunde die Zellmembran eines postganglionären Sympathikusneurons. Dort entsteht eine spezifische Bindung an Proteinmoleküle der postsynaptischen Zellmembran, wodurch die Acetylcholinrezeptoren sich an diese Moleküle anpassen. Bei einer Besetzung der Rezeptoren mit Acetylcholinmolekülen kommt es zu einer Aktivierung der Rezeptormoleküle und somit zu einer Beeinflussung der postganglionären Neuronen durch „Depolarisation“. Im Ruhezustand sind die Zellmembranen dieser Neuronen polarisiert, d.h. sie sind an ihrer äußeren Seite positiv, an ihrer inneren elektrisch negativ aufgeladen (Rüegg J C, 2003).
Die postganglionären Sympathikusneuronen werden durch den Einfluss von Acetylcholin elektrisch entladen und lösen daraufhin Aktionspotenziale aus. Diese werden vom Zellkörper des Neurons im sympathischen Ganglion in einer Geschwindigkeit von einem Meter pro Sekunde bis in die Nervenendigungen in den sympathisch innervierten Zielorganen fortgeleitet. Es kommt zu einer Ausschüttung von Noradrenalin, welches, wie schon Rüegg erklärt, an die adrenergenen bzw. noradrenergenen Rezeptoren der Zielorgane gebunden wird und eine noradrenerge Organreaktion auslöst, beispielsweise eine Gefäßkonstriktion, die auch dadurch zustande kommt, dass Noradrenalin die Gefäßmuskulatur über die Blutbahn erreicht.
Der Sympathikus und der Parasympathikus bestehen aus zweizelligen Neuronenketten (vgl. Abb. 7). In parasympathischen Ganglien findet die Verschaltung der prä- und postganglionären parasympathischn Neuronen statt. (Rüegg J C, 2003)
6.3 Das periphere vegetative Nervensystem
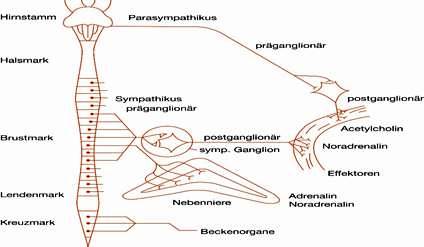
Abb. 7: Das periphere vegetative Nervensystem
Schematische Darstellung des peripheren Nervensystems.
Rechts: Zweizellige Neuronenkette im parasympathischen Vagusnerv.
Mitte: Schematische Darstellung des Verlaufs eines präganglionären Neurons des Sympathikus vom Rückenmark zum Mark der Nebennieren und zum postganglionären Neuron, welches das Zielorgan (z.B. Herz oder Blutgefäß) innerviert. Parasympathikus und Sympathikus beeinflussen die Zielorgane (Effektoren) durch Freisetzung der Neurotransmitter (Noradrenalin bzw. Acetylcholin). Das Nebennierenmark schüttet 80% Adrenalin und 20% Noradrenalin ins Blut aus.
Links: Hirnstamm und Rückenmark mit den Ursprungsgebieten des Sympathikus (Lendenmark und Brustmark) und des Parasympathikus (Kreuzmark und Hirnstamm). Modifiziert übernommen aus: Rüegg J C, 2003, S. 59
Acetylcholin ist auch hier, wie schon in den sympathischen Ganglien, für die Signalübermittlung zuständig. Dieser Neurotransmitter wird jedoch im Unterschied zum Sympathikus ebenso von den postganglionären parasympathischen Nervenendigungen an den Erfolgsorganen freigesetzt.
Wie schon Rüegg erklärt, erfolgt die Reaktion von Acetylcholin an den Erfolgsorganen und in den parasympathischen und sympathischen Ganglien mit zwei Typen von Acetylcholinrezeptoren, die in nikotinerg bzw. muskarinerg unterschieden werden. Nikotin und das Pilzgift Muskarin sind für diese Bezeichnungen zuständig, da diese für die spezifische Erregung der Acetylcholinezeptoren verantwortlich sind und somit pharmakologisch differenziert werden können. Die nikotinergen Acetylcholinrezeptoren sind im Körper weit verstreut, sowohl in den parasympathischen und sympathischen Ganglien, als auch in den willkürlichen Muskeln und ebenso im Gehirn. Dort vermitteln sie die stimulierende Wirkung des Nikotins.
Die muskarinergen Rezeptoren sitzen hauptsächlich an den Membranen der glatten Muskelzellen parasympathisch innervierter Organe. Die parasympathische Übertragung von postganglionären Neuronen auf Ziel- bzw. Effektororgane (z.B. die Pupille) werden durch Atropin komplett blockiert. Dieses giftige Tropan-Alkaloid bindet sich an die muskarinergen Acetylcholinrezeptoren und lässt die Wirkung des parasympathischen Überträgerstoffs Acetylcholin sinken. Da der Einfluss des Parasympathikus sinkt, gewinnt der Sympathikus an Bedeutung. Seltsamerweise hemmt Atropin nicht die gefäßerweiternde Wirkung des Parasympathikus beim männlichen Geschlechtsorgan. Somit wird angenommen, dass noch andere parasympathische Überträgerstoffe miteinbezogen sein müssen, vermutlich das Neuropeptid Vaso-intestinales Peptid (VIP) wie auch das Gas NO (Stickoxid). Viagra erhöht die entspannende Wirkung von NO auf die glatte Muskulatur des Schwellkörpers und verstärkt somit die Erektion beim männlichen Glied. (Rüegg J C, 2003)
6.3.1 Das Nebennierenmark stößt Adrenalin aus
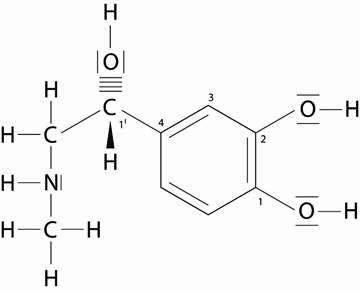
Abb. 8: L-Adrenalin: chemische Zusammensetzung von L-Adrenalin.
Modifiziert übernommen aus Löffler G, 2001, S. 481
Die Bildung von Adrenalin und Noradrenalin findet im Nebennierenmark statt. Beide sind wichtige Stresshormone. Adrenalin wird auch in bestimmten Nervenzellen, den sogenannten sympathischen Ganglien gebildet. Im Falle einer Ausschüttung von Adrenalin wird auch Noradrenalin in einer 4-fach geringeren Menge freigesetzt. Adrenalin zählt zu den wichtigsten Hormonen der Neurotransmitter und gehört auch zur Gruppe der Katecholamine. Dopamin bzw. Noradrenalin gehören ebenfalls dazu und haben eine ähnliche Wirkung. Bei Gefahr senden sie Signale aus. Wut und Furcht aktivieren den Sympathikus und der Adrenalinspiegel steigt bis ins 10-fache. Dadurch werden die Stoffwechselprozesse aktiviert und der Blutzuckerspiegel erhöht. Im Takt des Pulses schwankt auch der Blutdruck und steigt bei jedem Herzschlag auf seinen höchsten Wert (systolischer Blutdruck). Dies enspricht in etwa dem Druck einer 120 mm hohen Quecksilbersäule. Schliesslich senkt sich der Wert und erreicht seinen Tiefpunkt (diastolischer Blutdruck, ca. 80 mm Hg). Von einem krankhaften Blutdruck (Hypertonie) wird gesprochen, wenn die systolischen und diastolischen Blutdruckwerte in der Ruhephase 90 bis 140 mm Hg (Ausnahme bei älteren Menschen: 95 zu 160 mm Hg) übersteigen.
(Andrawis A, 2011)
Medikamente die eine hemmende Wirkung auf Adrenalin und Noradrenalin haben, führen zu einer Senkung des Blutdruckes.
6.3.2 Stress und hoher Blutdruck
Bei Gefahr oder Bedrohung aktiviert eine Signal- und Notfallreaktion den Sympathikus. Die Nebennieren reagieren darauf mit Ausschüttung von Adrenalin ins Blut. Demzufolge erhöht sich die vom Herzen strömende Blutmenge (das Herzzeitvolumen) und der systolische Blutdruck. Dies geschieht, wie schon Rüegg erklärt, durch die Erhöhung des Sympathikustonus, weil durch eine Verengung der Blutadern der Strömungswiderstand im Kreislaufsystem ansteigt. Im Falle eines neurogenen Hochdrucks tritt eine erhöhte Frequenz neuronaler Impulse in den sympathischen Nervenfasern auf. Bei gestressten Menschen ist der Noradrenalinspiegel erhöht und eine Verengung der Blutgefäße die Folge.
Der Grund ist die starke Reaktion der Gefäßmuskulatur auf Noradrenalin. (Rüegg J C, 2003)
Welche zellphysiolologischen und molekularen Mechanismen bewirken bei einer Überaktivierung des Sympathikus die bessere Signalübermittlung noradrenergen Synapsen zwischen Nervenendigungen und Blutgefäßen?
Wie schon Rüegg beschreibt, ist für die Transmitterfreisetzung die Reihenfolge der Impulse (Aktionspotenziale) in den postganglionären Nervenfasern von Bedeutung. Aus diesem Grund kommt es durch Einfluß des Sympathikus zur Erhöhung des Strömungswiderstands im Gefäß, wodurch der Blutdruck erhöht wird. (Rüegg J C, 2003)
Die Anzahl der Speicherbläschen in den Nervenendigungen ist für die Signalübermittlung von grosser Wichtigkeit. Wie schnell Neurotransmitter ersetzt werden und der Speicher nachgefüllt wird, spielt eine wichtige Rolle. Nur 80% des Noradrenalin können freigesetzt und in die Speicherbläschen zurückgepumpt werden. Die übrigen 20% werden durch eine neue synthetische Produktion ersetzt. Durch Stress verursachte Disharmonie zwischen der Aktivierung des Noradrenalinspiegels und der Transmitterproduktion über die Sympathikusfasern erfolgt eine Veränderung im Blutplasma. (Rüegg J C, 2003)
Wie schon Rüegg erklärt, kommt es zur Freisetzung von Neuropeptid Y (NPY) (Acetylcholin und peptidische KO-Transmitter) in den präganglionären Nervenendigungen. Neuropeptid Y bewirkt die vermehrte Bildung von zyklischem Adenosinmonophosphat (cAMP), einem intrazellulären Botenstoff in den postganglionären Neuronen. Dieser führt zu einer Aktivierung der Proteinkinase, einem Enzym, das eine Phosphatgruppe von Adenosintriphosphat (ATP) auf das Tyrosinhydroxylasemolekül überträgt. ATP verursacht den Phosphorylierungsprozeß. Das Resultat ist eine optimale Regulation der Synthese von Noradrenalin und eine Anpassung des Gehalts des verfügbaren Transmitters an die wechselnden Bedingungen neuronaler Aktivität. (Rüegg J C, 2003)
Dieser Regulationsmechanismus spielt sich nicht nur in den adrenergen Neuronen des Zentralnervensystems (ZNS), sondern auch in den sympathischen Ganglien ab. Infolgedessen ist auch die zerebrale adrenerge Signalübermittlung bei Stress und im Gehirn die Tyrosinhydroxylreaktivität langfristig verstärkt. Durch den Botenstoff cAMP wird im Stressfall bei chronisch erhöhtem Sympathikustonus nicht nur die enzymatische Aktivität der Tyrosinhydroxylreaktivität erhöht, sondern auch die Expression eines Erbfaktors des Hydroxyülase-Gens im Zellkern, welche für die Produktion des Enzyms verantwortlich ist.
So steigt die Anzahl der Enzymmoleküle in den Nervenzellen und es erhöht sich der Noradrenalingehalt in den Speicherbläschen der postganglionären Neuronen. Dieser Zustand bleibt für einige Tage erhalten.
Die Nachwirkung von Stress hält sich langfristig. Somit wird bei jedem Nervenimpuls an den sympathischen Nervenenden mehr Noradrenalin ausgeschüttet als je zuvor und die Signalübertragung vom Sympathikus auf die glatte Muskulatur wird verbessert. Der Blutdruck steigt an. In den postganglionären Sympathikusneuronen haben aktivitätsabhängige Veränderungen Auswirkungen auf die neuronale Plastizität des ZNS bzw. sympathischen Nervensystems.
Auch im Gehirn verstärkt sich bei Stress die Expression (Synthese) der Tyrosinhydroxylase. (ebd.).